2025/7/21公開 著者:愛知医科大学病院 薬剤部 山本絵理子
第208回愛知医科大学病院NST勉強会 講演アーカイブ
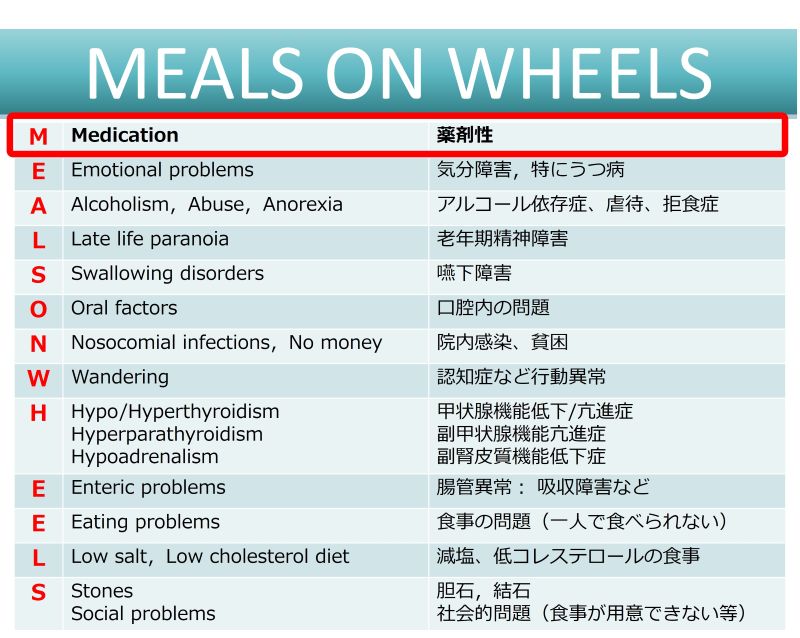
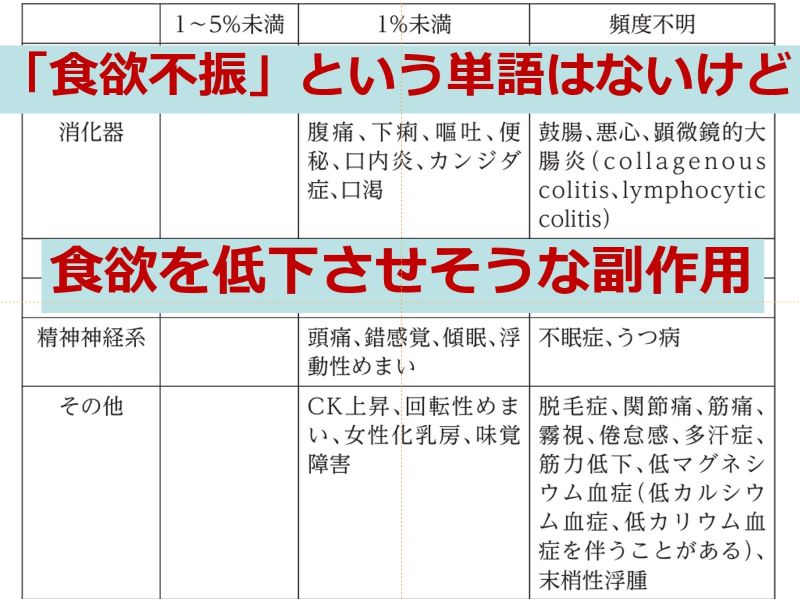
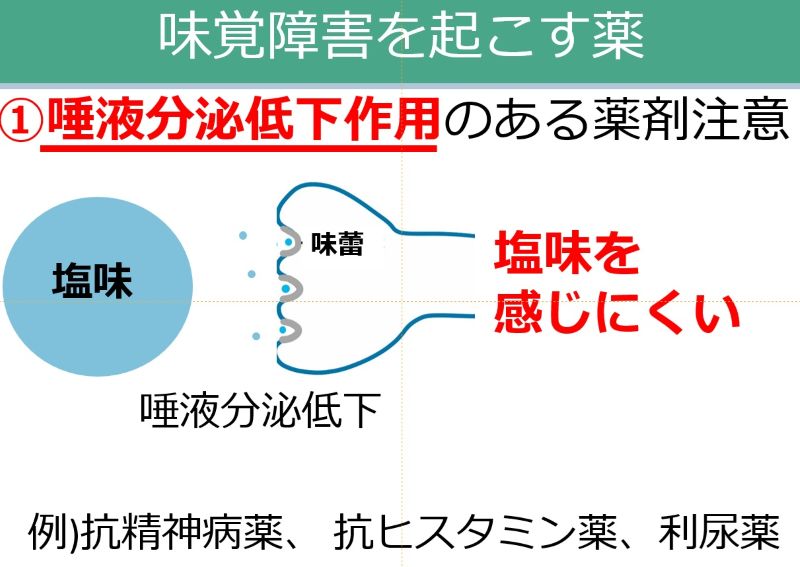
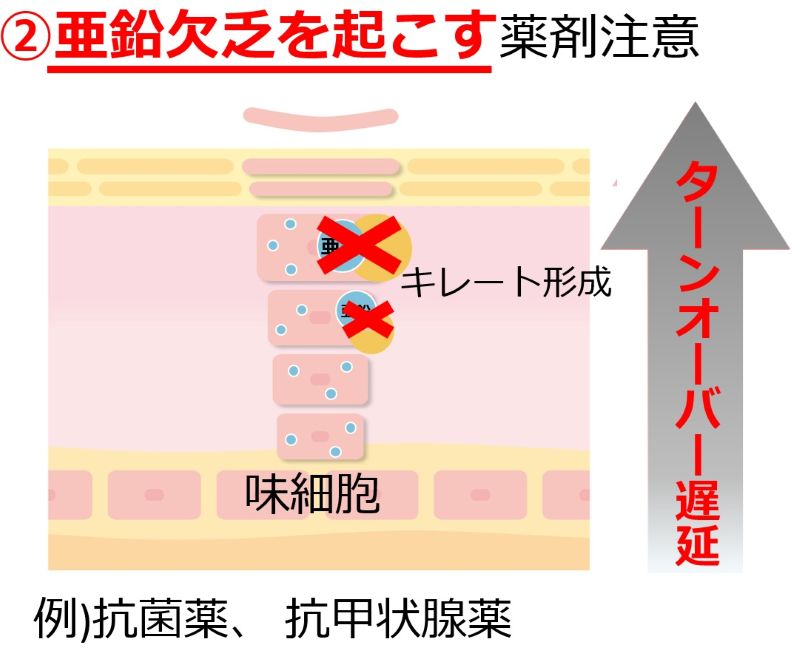
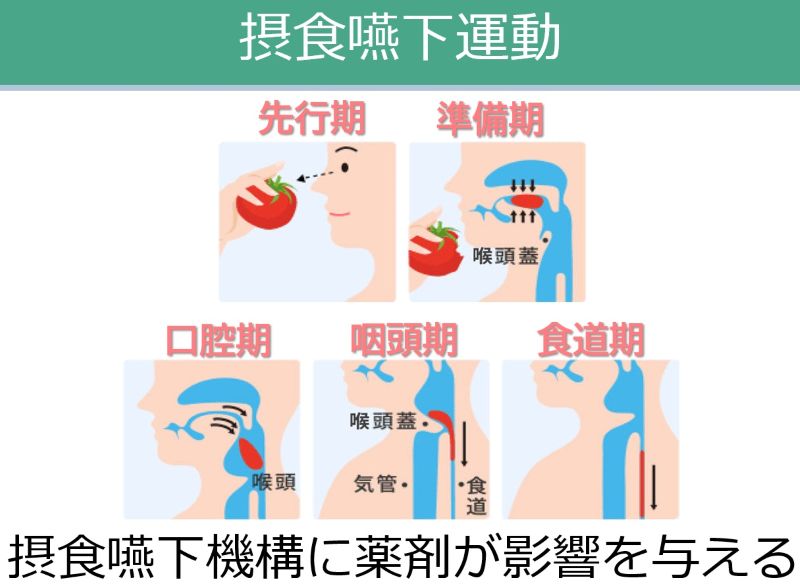
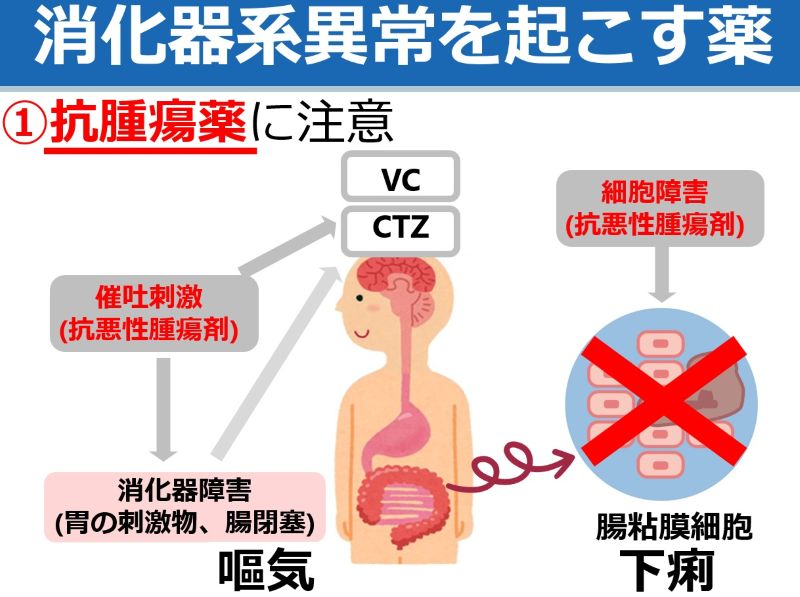
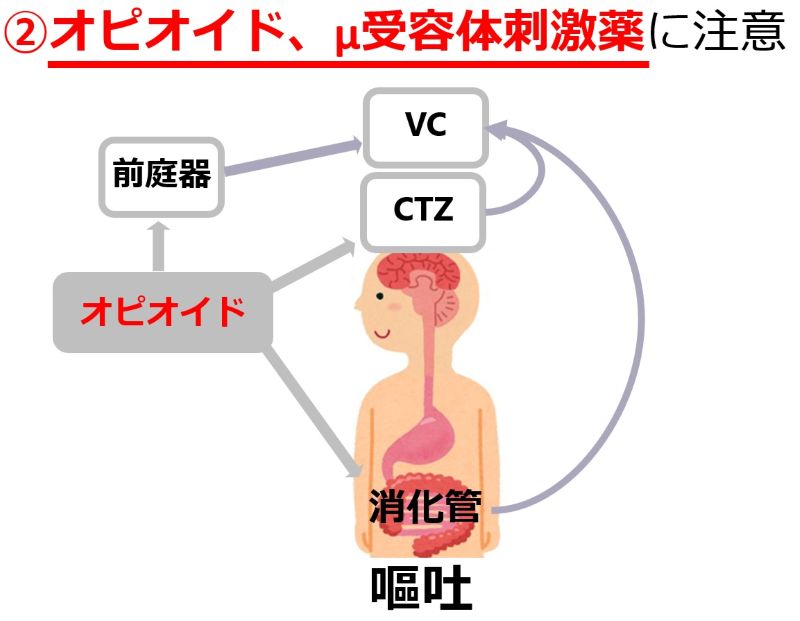
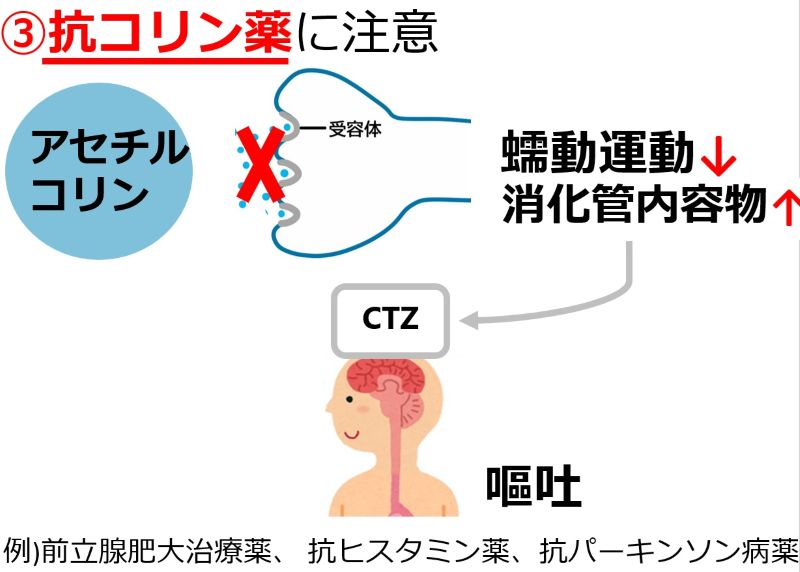
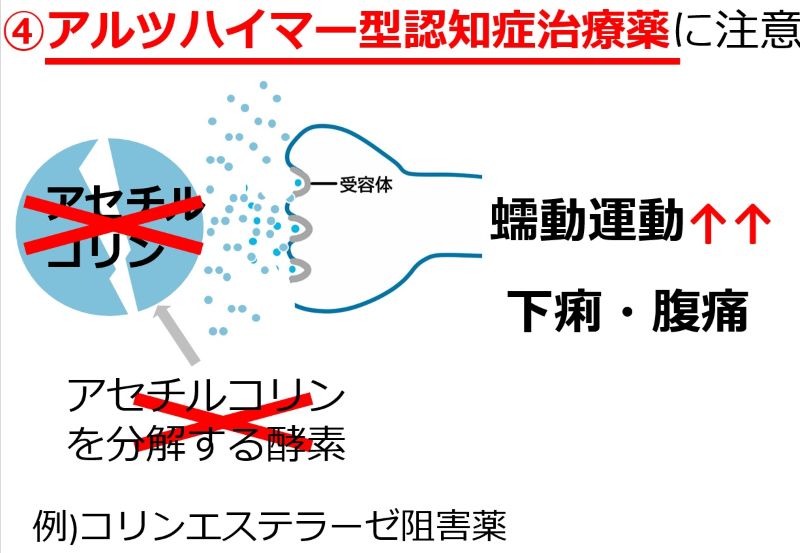
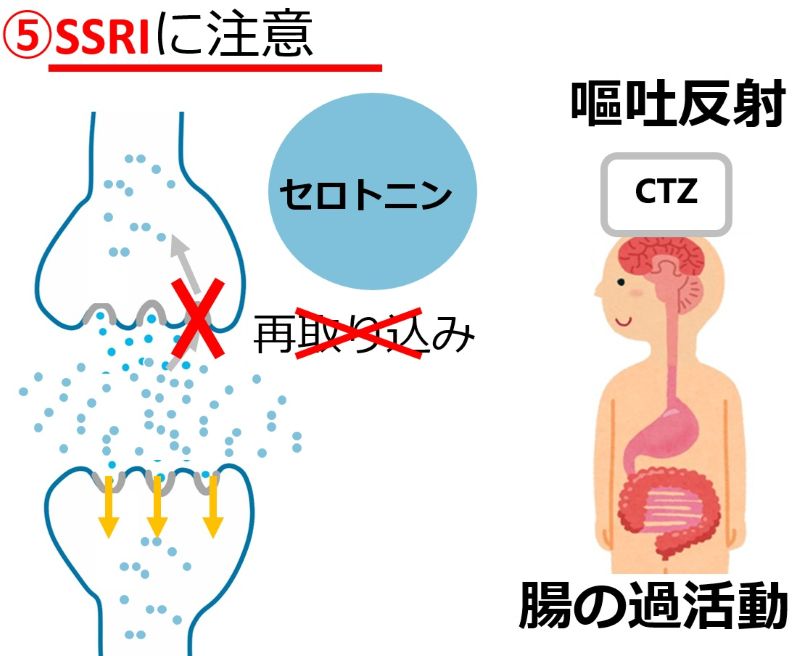
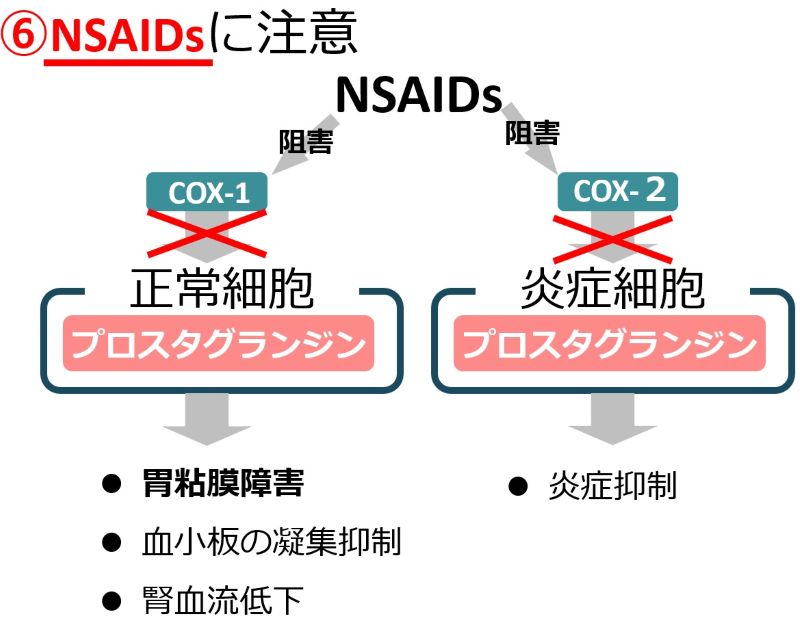
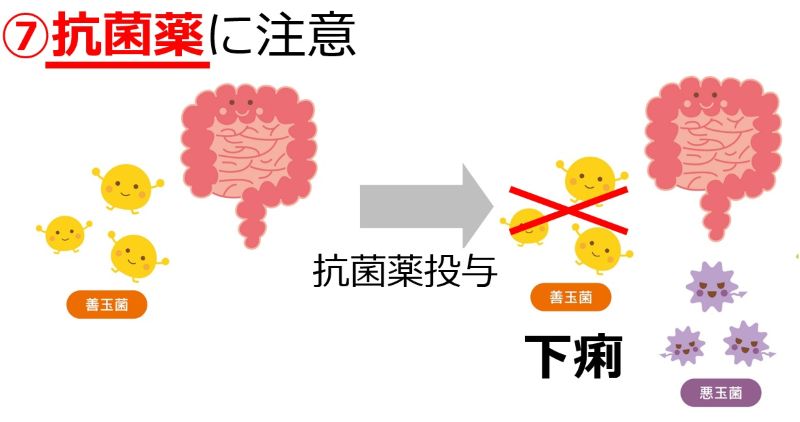
| 食欲に影響する薬:知っておきたい5つのポイント • 多くの薬が食欲不振を引き起こす可能性があり、低栄養や入院期間延長のリスクを高めます。 • 薬による食欲不振は、口腔・嚥下、消化器、精神神経系など多岐にわたるメカニズムで発生します。 • 食欲不振の原因となっている薬の特定が重要です。休薬・減量・変更を検討しましょう。 • 薬剤師は薬の副作用特定を助ける専門家です。症状出現時期で原因薬を探しやすくなります。 |